Morales
destacó que este proyecto se constituye en la primera planta petroquímica del
país con la más grande inversión de 2.200 millones de dólares.
De
acuerdo al proyecto, el complejo estará compuesto por plantas de propileno y
polipropileno, y procesarán 250.000 toneladas métricas por año de
polipropileno, que tendrá como mercado objetivo, según el estudio de Ingeniería
Conceptual: Brasil, Argentina, Perú, Bolivia y China. Entre el 10 y 20%
estará destinado para el mercado interno y entre el 80 y 90% al mercado
externo.
Entre
los beneficios, el complejo generará 4.000 empleos directos en la fase de
construcción; además de 150 empleos directos y 10.000 indirectos en la fase de
operación con un efecto multiplicador en el sector manufacturero.
Las
plantas de propileno y polipropileno se alimentarán de propano, materia prima
que proviene de la Planta de Separación de Líquidos “Carlos Villegas”;
permitirá la manufactura de productos en base de polipropileno, generación de
fábricas, producción de envases plásticos, tuberías, nylon, sacos de
tejidos (saquillos) y bolsas para productos industriales.
La
industria privada y estatal tendrá acceso a una materia prima nacional a bajo
costo y se estimularán las inversiones y el desarrollo industrial.
El
complejo supone el mayor salto industrial para Bolivia, además, por la venta de
polipropileno el país captará $us 420 millones por año.
La
construcción de la planta petroquímica de propileo - polipropileno, junto a la
de etileno - polietileno son parte de la política de industrialización de los
hidrocarburos que lleva adelante el Gobierno nacional.
El
polipropileno es uno de los polímeros más versátiles y de bajo costo en la
industria. Sus aplicaciones varían desde productos como películas utilizadas en
el embalaje de alimentos para refrigerios, hasta elementos de mayor valor, como
aparatos de uso doméstico, productos electrónicos y partes automotrices
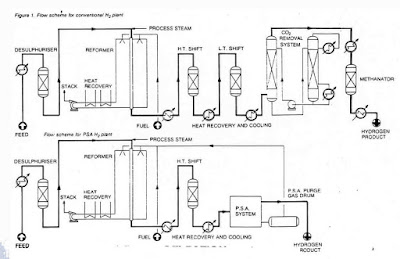
La
materia prima es obtenida a partir de la planta criogénica como se muestra en
el siguiente diagrama de procesos:
GAS NATURAL
El principal componente es
el metano (superior al 90%)
• El
etano es un excelente precursor (materia prima) de la
• Principal
olefina (etileno)
• Propano
y butanos GLP son cortes de menor uso petroquímico
• Las
refinerías producen GLP insaturado (propileno y butilenos)
• Propileno
y butilenos son considerados petroquímicos básicos
• La
producción petroquímica a partir de gas natural requiere la
• Separación
física de sus principales componentes
Gas de síntesis
• Es
una mezcla de hidrogeno, monóxido y dióxido de carbono
• Se
obtiene por el proceso de reformado al vapor
• La
materia prima suele ser metano (también etano, lpg, etc)
• La
unidad principal es el horno de reforming
• Las
unidades adicionales dependen del uso del gas de síntesis
• Los
principales derivados petroquímicos son metanol y
Amoníaco
ESQUEMA UNIDAD DE GAS DE
SÍNTESIS
• Se
obtiene por reacción de hidrógeno y monóxido de carbono
• La
capacidad mundial instalada alcanza los 60 millones ton/año
• Gran
capacidad instalada en américa latina: trinidad y tobago,
• Chile
• En
argentina el principal productor es ypf (400 m ton/año)
• Usos
principales: formaldehido, mtbe, ácido acético, biodiesel
• Producto
líquido de fácil transporte (exportación)
• Aumento
significativo de la capacidad (+10 mm ton/año) en 2010
ESQUEMA UNIDAD DE METANOL
Usos del metanol
• El
formaldehído se obtiene por oxidación de metanol
• Se
utiliza en la elaboración de resinas termoestables, por
• Reacción
con fenol, urea o melamina
• Un
tercio de la producción mundial de metanol se destina a
• Formaldehído
• Segundo
uso del metanol (25%) es la elaboración de mtbe
• El
mtbe (metil etil eter) es un buen antidetonante (octanaje)
• Nuevo
uso del metanol es la elaboración de biodiesel
Amoníaco
• Se
obtiene por reacción del hidrógeno con nitrógeno
• La
capacidad mundial instalada alcanza los 180 millones ton/año
• El
50% de la capacidad mundial está en asia (china, india, etc)
• En
argentina dos productores: profertil y bunge (ex
• Petrobras)
• Uso
principal: fertilizantes (urea, otros nitrogenados)
• Profertil
produce amoníaco y urea en argentina con
• Capacidades
de 0,75 y 1,1 mm ton/año respectivamente
ESQUEMA UNIDAD DE AMONÍACO
• La
capacidad mundial instalada alcanza 150 millones ton/año
• 50%
capacidad mundial en asia, al igual que amoníaco
• En
argentina mismos productores que urea (profertil, bunge)
• Usos:
fertilizantes, resinas ureicas (plásticos)
• Principal
aporte de nitrógeno a los suelos, a veces como una (urea - nitrato de amonio)
Esquema unidad de urea
• El
etileno es la principal olefina en volumen a nivel mundial
• La
capacidad mundial instalada alcanza los 130 millones ton/año
• Existen
varias materias primas en su elaboración
• Las
principales son etano (del gas) y nafta virgen (del petróleo)
• La
planta de producción etileno es el cracker térmico
• A
partir de etano se produce principalmente etileno
• A
partir de nafta virgen se obtiene además de etileno, propileno,
·
Butilenos, butadieno y
gasolina de pirólisis (aromáticos)
ESQUEMA DE CRACKER TÉRMICO
• La
capacidad de etileno en américa latina es de 6,7 mm ton/año
• Representa
5% de la capacidad mundial instalada (130mm ton/año)
• Brasil
es el mayor productor con 6 crackers y 3,7 mm ton/año
• Argentina
posee 4 crackers, los dos mayores en bahía blanca Con 700 m ton/año
• Venezuela
y méxico poseen 0,6 y 1,5 mm ton/año respectivamente
• La
mayoría de los crackers operan con etano (materia prima); solo brasil posee
mayoría de crackers a base de nafta virgen
Usos del etileno
• El
principal derivado es el polietileno (pe)
• Existen
varios tipos de pe: baja densidad (pebd) , alta densidad (pead) y polietileno
lineal de baja densidad (pelbd)
• Los
principales productores de pe son los mismos que etileno: Braskem, dow, pemex,
pequiven
• Segundo
uso en importancia es el pvc
• Tercer
uso es el óxido de etileno y su derivado etilenglicol
• Otros
usos de etileno: estireno y su derivado poliestireno
Propileno
• Hay
varias vías de obtención además del craqueo térmico
• La
segunda en importancia es el cracking catalítico (fcc)
• Dos
vías recientes: deshidrogenación de propano y metátesis
• El
principal derivado de propileno es el polipropileno (pp). Su
• Demanda
mundial viene creciendo a altas tasas en el mundo
• Otros
derivados importantes: acrilonitrilo, óxido de propileno
• Los
crackers de etano producen muy poco propileno
Oferta y demanda regional
• Existe
importante capacidad de producción de gas de síntesis en América latina no sólo
para derivados petroquímicos (metanol, Amoníaco-urea), sino otros usos
(hidrógeno, siderurgia, etc)
• En
el caso del metanol la oferta (excluye trinidad y tobago) 6,5 Mm ton/año supera
netamente a la demanda (1,5 mm ton/año) • para el amoníaco la oferta y la
demanda son similares, ambas de Aproximadamente 1,5 mm ton/año, con algún
deficit en Brasil en urea la mayor capacidad está en Venezuela (2,5 mm
ton/año); Brasil con apenas 1,1 mm ton/año importa 75% de su consumo
•
la capacidad de etileno en américa latina está integrada con la Producción de
derivados (polietileno, pvc, óxido de etileno, etc) la región es deficitaria en
polietilenos en 2 millones ton/año Siendo en gran medida méxico y en menor
chile los importadores • la capacidad de pvc es de 2 millones ton/año y el
deficit de 0,3 mm Ton/año es básicamente de brasil. México y colombia tienen Capacidad
importante de pvc. el oxido de etileno y su derivado principal: etilenglicol,
se Produce en méxico y brasil principalmente eletilenglicol, cuyo destino
principal es el pet, es deficitario En argentina (no se produce) e insuficiente
en brasil y méxico
•
en casi toda américa latina el propileno se obtiene en las Refinerías (fcc)
sólo en brasil se obtienen además volúmenes importantes de Propileno en
crackers térmicos al usar estos nafta virgen el polipropileno, principal
derivado del propileno, se Produce en argentina, brasil, chile, colombia,
méxico y Venezuela la capacidad de la región es de 2,5 millones ton/año • el
principal importador neto es méxico con 0,6 mm ton/año y le Sigue perú (125 m
ton/año). Argentina y brasil están Equilibrados.
Mercado Internacional PP y el Polipropileno
Mercado Internacional PP y el Polipropileno
En
un estudio realizado en el 2011 de una empresa de investigación alemana de
nombre Ceresana ubicada en Alemania meridional pronostica un desarrollo
dinámico de la demanda mundial de propileno, es decir, un aumento de más
de 20 millones de toneladas en 2017. Ellos indican que "Las ventas de
propileno alcanzaron su valor máximo de más de 90 mil millones de dólares
EE.UU. en 2008", informa Oliver Kutsch, el presidente del instituto de
investigación de mercado. "Este nivel será superado tan pronto como en
2012".
Un
factor importante, que tendrá un impacto en el mercado mundial de propileno, es
la expansión de la capacidad masiva de propileno y productos derivados en
el Medio Oriente y China. Países del Medio Oriente presentan
los mayores incrementos en la producción de propileno y la demanda. Se espera
que la oferta y la demanda en esos países se habrá duplicado para el año 2014.
Sin embargo, el Asia-Pacífico región seguirá dominando el mercado y generar
más del 45% de toda la demanda.
El
mercado del propileno segundo se compone de productores de acrilonitrilo,
seguido por óxido de propileno. El acrilonitrilo es usado principalmente
para la producción de fibras acrílicas, las cuales son procesadas en los
textiles. Los derivados de óxido de propileno son necesarios como
materias primas para la fabricación de productos como el poliuretano, lacas y
adhesivos, resinas de poliéster, refrigerantes, anticongelantes y disolventes.
El estudio, elaborado por Ceresana
Investigación analiza el mercado mundial de propileno: demanda,
producción, importaciones, exportaciones, los ingresos y los precios son
examinadas, incluyendo las previsiones hasta el año 2017. Se hace especial
hincapié en los 55 países donde se produce propileno. Las áreas investigadas a
fondo las aplicaciones son el polipropileno, acrilonitrilo, óxido de propileno,
cumeno, isopropanol, ácido acrílico, 2-etilhexanol, y n-butanol. La guía de los
compradores de las listas de útiles 137 perfiles de todos los fabricantes
grandes de propileno.
Demanda y Oferta Mundial
El
consumo mundial de polipropileno aumentó en casi 7 por ciento, o 2,2 millones
de toneladas, para alcanzar un total de 34 millones de toneladas métricas en
2009. El informe anual 2010 PTAI para el polipropileno estima que la
demanda global para el polipropileno creció otro 7 por ciento global en 2010 y alcanzará cerca de 36,4
millones de toneladas.
Un factor importante, que tendrá un
impacto en el mercado mundial de propileno, es la expansión de la capacidad
masiva de propileno y productos derivados en el Medio Oriente y China. Países del Medio Oriente presentan los mayores incrementos
en la producción de propileno y la demanda. Se espera que la oferta y la
demanda en esos países se habrá duplicado para el año 2014. Sin embargo, el Asia-Pacífico región seguirá dominando el mercado y
generar más del 45% de toda la demanda.
Asia, y China en particular, han tenido
un crecimiento en el consumo del polipropileno difícil de entender. Como
consecuencia del pobre crecimiento, los planes de la expansión en las regiones
desarrolladas se están echando atrás; ahora, solo se están implementando,
planes de reducción de costos. El buen y continuo crecimiento en otras
regiones significa que se van a anunciar nuevos planes de
expansión.
India es otro país donde el consumo de
polipropileno está creciendo rápidamente, incluso más rápidamente que China ha
mencionado Smith. India agregará otras 0,4 millones de toneladas de
polipropileno a su capacidad en los próximos cinco años.
La región del Oriente Medio y
África también está parada en su consumo, pero sus incrementos de capacidad
están creciendo mucho más rápido que en otras regiones. El aumento de esta
capacidad podrá ser utilizada para resolver otras demandas regionales lo que
permitirá aumentar sus exportaciones de polipropileno durante los próximos
cinco años.
Mercado Nacional del PP y el Propileno.
La
proyección del consumo de poliolefinas El mercado es claramente dominado por el
polietileno. Los productos derivados del polietileno son sumamente variados,
junto al PVC y el PP, son los denominados comodines , aquellos que por ser producidos
en tan alta cantidad, su precio es sumamente bajo, alrededor 700$/ton.
La
tasa de crecimiento del Polipropileno y Polietileno, es igual, y generalmente
el polipropileno tiene una tasa de crecimiento mayor al polietileno. El
crecimiento del PE esta ligado al crecimiento del PIB de una nación, mientras
que el PP es un poco más innovativo, buscando nuevos mercados a través de
nuevas aplicaciones (el gran consumidor de PP son las empresas automotrices.
Demanda y Oferta Nacional .
La
tasa de crecimiento del Polipropileno y Polietileno, es igual, y generalmente
el polipropileno tiene una tasa de crecimiento mayor al polietileno. El
crecimiento del PE esta ligado al crecimiento del PIB de una nación, mientras
que el PP es un poco más innovativo, buscando nuevos mercados a través de
nuevas aplicaciones (el gran consumidor de PP son las empresas automotrices.
PRODUCCIÓN
DE POLIPROPILENO
Introducción
El polipropileno (PP) –(C3H6)–n es un
polímero termoplástico que se obtiene de la polimerización del propileno (o
propeno). El polipropileno es un polímero de adición ya que se produce por un
mecanismo en el cual el monómero se agrega en el extremo de crecimiento de la
cadena. Este mecanismo también suele llamarse polimerización por crecimiento de
cadena y es típico de las olefinas. Las propiedades del polipropileno, como la
de todos los polímeros, dependen de muchas variables entre las que se
encuentran el grado de cristalinidad, el tipo de polimerización, etc. La
mayoría de ellas corresponden a polipropileno isotáctico obtenido mediante
catalizadores Ziegler-Natta. El polipropileno isotáctico
cristaliza en forma helicoidal, con tres grupos –CH3 por paso. Es lineal,
altamente cristalino, de alto peso molecular y sin insaturaciones. Presenta
propiedades análogas al polietileno, pero el grupo –CH3 aumenta la rigidez de
la cadena (mayor temperatura de fusión) e interfiere la simetría molecular. Su
densidad se encuentra en torno a 0,90 g/cm3, lo que lo hace el más ligero de
los plásticos importantes. Su alta cristalinidad le proporciona una elevada
resistencia a la tracción, rigidez y dureza. Posee excelentes propiedades
eléctricas, carácter químico inerte y resistencia a la humedad. Se halla
completamente libre de cuarteamiento por tensiones ambientales.
No obstante, es menos estable al
calor, la luz y los ataques oxidantes que el polietileno y debe estabilizarse
con antioxidantes y absorbentes de luz ultravioleta para que su procesado y
comportamiento a la intemperie sean satisfactorios. El polipropileno es un
polímero ampliamente utilizado en diversas aplicaciones. A continuación se
detallan algunas de ellas: Autopartes: paragolpes, torpedos, alerones,
guardabarros, volantes, pedales de acelerador (con bisagra tipo film),
conductos de calefacción y refrigeración, carcasas de filtros de aire, cajas de
baterías, etc. 2
Artículos
domésticos: baldes, bisagras de muebles, respaldos
de sillas, botellas y tapones, cubertería, aparatos de cocina, carcasa de
electrodomésticos, juguetes, tejidos para alfombras, vasos, etc. Electrotecnia:
carcasa de transformadores, cubierta de cables, láminas de capacitores,
accesorios de antenas, etc. Construcción: tuberías de desagüe y codos,
depósitos de agua caliente, radiadores, etc. Medicina: aparatos médicos
esterilizables, jeringas desechables, recipientes de transfusión, etc. Otros:
césped sintético, pistas de esquí en verano, tacones de zapatos, cordeles,
papeles de embalaje, maletas, cajas de herramientas, carcasas de bombas, etc.
Obtención
del monómero (propileno)
Craqueo con
vapor
En
el craqueo con vapor, una mezcla de hidrocarburos (etano, GLP,
naftas o gas oil) y vapor se precalienta hasta 600 ºC en la sección convectiva
de un horno de pirolisis. Luego, se calienta aún más en la sección radiante
hasta como mucho 900 ºC. El vapor reduce la presión parcial del hidrocarburo en
el reactor. La relación másica entre el vapor y el hidrocarburo es generalmente
función de la alimentación y varía desde 0,2 para el etano hasta más de 2,0
para gas oils. La cantidad de vapor utilizado es elegida optimizando el
rendimiento (la selectividad de la olefina), el consumo de energía y la
longitud del horno, limitada por la coquificación. El tiempo de residencia
varía entre 1 s, en las plantas antiguas, hasta un mínimo de 0,1 s, en algunos
hornos nuevos. El tiempo de residencia determina la selectividad de la olefina.
En un tren de separación de olefinas, el propileno se obtiene por destilación
de una corriente mezcla de C3, que contiene propano, propileno y otros
componentes minoritarios. En la torre C3, el propileno se separa por cabeza de
la columna, mientras que por fondo se separa una mezcla rica en propano. El
tamaño de la columna varía según el grado de pureza buscado para el propileno.
Se requiere mayor número de platos para el propileno de grado polímero.
Deshidrogenación
de propano
El
aumento de la demanda a partir de los años „80, especialmente por la expansión
del polipropileno, superó la disponibilidad de las fuentes clásicas y motivó el
desarrollo de un proceso dedicado exclusivamente a producir propeno, así fue
como surgió la deshidrogenación de propano del GLP. La deshidrogenación del
propano es una reacción de equilibrio endotérmica que se lleva a cabo en
presencia de un catalizador de un metal pesado o noble como platino o cromo. C3H8
C3H6 + H2 Este proceso es altamente selectivo, el rendimiento global de
propileno es de alrededor de 90%. Aumentos en la temperatura y disminuciones de
la presión aumentan el rendimiento como indica el principio de Le Chatellier.
Sin embargo, el aumento de la temperatura genera pirolisis del propano y
formación de coque que desactiva el catalizador. Por lo que las condiciones
operativas típicas son presión cercana a la atmosférica y temperaturas entre
500 – 700 ºC. Existen numerosas tecnologías de deshidrogenación de propano.
Algunas de ellas son: Oleflex (UOP), Catofin (Air
Products And Chemicals) y STAR (Philips Petroleum). El proceso Oleflex
utiliza un catalizador de platino sobre alúmina. Consiste en cuatro
reactores adiabáticos con enfriamiento intermedio en serie. El rendimiento es
superior al 85%.
Proceso Oleflex
Catalizadores
y cinética
Tipo de
catalizador
La
mayor parte de las poliolefinas se obtienen industrialmente mediante
polimerización por coordinación, utilizando catalizadores heterogéneos Ziegler-Natta.
Un catalizador Ziegler-Natta puede ser definido como un compuesto
de un metal de transición que mediante un enlace metal – carbono es capaz de
realizar la inserción repetitiva de unidades olefínicas. Generalmente, el
catalizador consiste de dos componentes, por ej. Una sal de metal de
transición, más frecuentemente un haluro (TiCl4 o TiCl3), y alquilo metálico,
como activador o cocatalizador (Al(C2H5)3 o Al(C2H5)2Cl), que tiene el
propósito de generar el enlace metal – carbono activo. El modelo de
Cossee – Arlman del sitio de polimerización sostiene que el sitio
activo es un átomo de un metal de transición coordinado octaédricamente, con un
sitio de coordinación vacante. En el caso del TiCl3, el sitio se forma por
reacción con el alquilaluminio. La inserción del monómero (propileno) ocurre
por un paso de coordinación del mismo con el metal de transición (Ti), formando
un complejo Ti – alqueno, luego se produce el debilitamiento del enlace Ti – C,
y finalmente la inserción. Subsecuentemente, el sitio vacante y la cadena en
crecimiento intercambian posiciones porque estas no son equivalentes en la red
cristalina del catalizador. Estas fases se repiten en la inserción de cada
molécula de monómero.
Mecanismo de polimerización catalítica
La
característica distintiva de estos catalizadores es su habilidad de producir
polímeros estereoregulares, ya que la quimisorción del monómero debería siempre
llevar a la misma orientación de la molécula sobre la superficie del
catalizador. La introducción de otros aditivos en el complejo catalítico, como
algunas bases de Lewis, especialmente ésteres aromáticos como el benzoato de
etilo, mejoraron sustancialmente la actividad y la estereoespecificidad. No
obstante, la mayor parte de la sal de titano era inactiva, por lo que tenía que
ser eliminada del sistema, con un incremento sustancial de los costes del
proceso. Con el desarrollo de catalizadores basados en TiCl4 se consiguió una
elevada estereorregularidad para el polipropileno, suprimiendo los costes de
separación del catalizador inactivo, ya que estos catalizadores presentaban
además altas actividades catalíticas. Al contrario que los catalizadores
heterogéneos, los cuales presentan centros activos con diferente
estereoselectividad, los catalizadores homogéneos tienen una estructura
molecular definida. Esto permite no sólo la producción de polímeros
extremadamente uniformes con distribuciones estrechas de pesos moleculares,
sino también correlacionar la actividad y la estereorregularidad con la
estructura molecular del catalizador.
Cinética de la reacción
La cinética de la polimerización del
propeno no es sencilla, ya que a medida que transcurre la polimerización, los
cristalitos de TiCl3 se rompen en pedazos más pequeños, generando nuevos
centros activos. Sin embargo, para la mayoría de los sistemas catalíticos, se
ha encontrado que la velocidad de polimerización es 7
proporcional
a las concentraciones del catalizador y del monómero, pero no depende del
compuesto orgánico de aluminio siempre y cuando se mantenga el umbral de
concentración.
Rp
= kp [C*] [C3H6] Donde: kp: Constante de propagación [C*]: Concentración de
sitios activos (proporcional al peso de catalizador) [C3H6]: Concentración de
propileno Esto significa que prácticamente no existe dependencia de la
velocidad de polimerización con la relación Al(C2H5) / TiCl3 en un amplio
rango.
Tecnología de producción de
polipropileno
Procesos comerciales de obtención de
polipropileno (Descripción e impacto tecnológico)
Proceso en suspensión (Slurry)
El
proceso en suspensión o slurry se utilizó principalmente en las décadas del „60
y „70. Se requería el empleo de un solvente como butano, heptano, hexano o
incluso parafinas más pesadas. El solvente cumplía el papel de medio de
dispersión del polímero producido en los reactores y disolvía el alto nivel de
polímero atáctico en su separación. El uso de solvente también facilitaba la desactivación
del catalizador y su extracción, que involucraba el contacto del producto del
reactor con alcohol y soluciones cáusticas. El proceso Montecatini (Montedison)
fue el primer proceso industrial, y sigue siendo el más representativo. Se
distinguen las siguientes etapas: Preparación del catalizador; polimerización;
recuperación de monómero y solvente; remoción de residuos de catalizador;
remoción de polipropileno atáctico y de bajo peso molecular; secado del
producto; adición de modificadores y extrusión del polímero. El sistema
catalítico consiste en TiCl3 con monoclorodietilaluminio, Al(C2H5)2Cl, en
solución en heptano. El TiCl3 se prepara primero por reducción de tetracloruro
de titanio con trietilaluminio, en un reactor agitado de acero inoxidable, y
luego se introduce al reactor de polimerización.
El
propileno se polimeriza en estado líquido a temperatura entre 60 y 80 ºC, y
presión entre 5 y 12 atm. El proceso de polimerización es continuo, se realiza
en heptano y se utiliza hidrógeno para reducir el peso molecular. El lodo
(slurry) que contiene el polímero se pasa a un reactor donde se separa parte
del propileno no reaccionado, se purifica y recicla; el catalizador se
descompone por reacción en metanol, en presencia de HCl anhidro, y se
neutraliza con solución de KOH al 50%. Los solventes se eliminan por
centrifugación. La mezcla de agua, metanol y heptano conteniendo el polímero
atáctico se envía a una columna en la cual los solventes son arrastrados por
vapor. El polímero atáctico se recupera por el fondo de la columna. El polímero
suspendido en agua se centrifuga y se transfiere a un secador. Una vez seco, se
mezcla con aditivos (antioxidantes en particular), se extruye en forma de
gránulos y se almacena en silos.
Proceso Montecatini
Proceso en masa con monómero en fase
líquida
La principal diferencia de este
proceso con respecto al de suspensión es la sustitución del solvente por
propileno líquido. Esto fue posible debido a que con el desarrollo de nuevos
catalizadores ya no fue más necesaria la extracción de catalizador ni la
remoción del polímero atáctico. 9
El
proceso Spheripol o Hypol (Mitsui Petrochemical) dependiendo de
sus diferentes versiones, es continuo y se basa en un catalizador superactivo
(Ti/MgCl2, un alquilaluminio, un donador de electrones).
En
un reactor tipo bucle la mezcla reaccionante fluye impulsada por una bomba
axial (no requiere agitación externa); alcanza alta velocidad lo que previene
la deposición de polímero en las paredes del reactor; el área de transferencia
de calor por unidad de volumen es más alta que en un reactor agitado, lo que
permite un mejor control de temperatura y mayor productividad. El tiempo de residencia
en el reactor se puede alterar, variando la velocidad de recirculación. El
propileno, que se puede diluir en propano (hasta el 40%), se alimenta al
reactor en presencia de catalizador e hidrógeno. La temperatura de reacción es
de entre 65 y 80 ºC, y la presión de 33 atm. La mezcla de reacción circula
rápidamente, y contiene hasta 50% de sólidos. Polímero y monómero no
reaccionado se separan en un tanque flash a 16 atm. El monómero se recircula al
reactor, y se remueve el propano sobrante. Al reactor de lecho fluidizado
ingresan las partículas de polímero y vapor de agua, con el fin de desactivar
el catalizador. El secado se realiza con nitrógeno. El polímero se obtiene en
forma de partículas esféricas con diámetro entre 1,5 y 2 mm y distribución de tamaño
estrecha. La productividad es del orden de 20 kg / g catalizador soportado
(1000 Kg / g Ti). El índice de isotacticidad es de 97%. El peso molecular se
controla por adición de hidrógeno durante la reacción, y también utilizando
compuestos organometálicos derivados de cinc o cadmio. Existen dos reactores en
serie: el primero para trabajar en masa y el segundo en fase gas. El primer
reactor es de tipo bucle, en el cual se hace circular catalizador y monómero a
gran velocidad para que permanezcan en suspensión en el diluyente. El diluyente
es en realidad el propio propileno líquido, el cual, dadas las condiciones de
operación, facilita la evacuación el calor generado por la reacción y al mismo
tiempo permite aumentar el rendimiento del sistema catalítico.
En
el segundo reactor, el de fase gas, se incorpora el polímero producido en el
reactor tipo bucle. En esta fase se preparan copolímeros con características
especiales añadiendo un comonómero (por ejemplo etileno) además del monómero.
Tras separar el polímero fabricado de las corrientes de propileno, y de
desactivar el catalizador, el polvo de polipropileno obtenido se envía a la
línea de acabado donde se añaden aditivos y se le da la forma requerida para su
distribución comercial.
Proceso Spheripol
El
proceso LIPP-SHAC (Shell) deriva su nombre de Liquid Propylene
Polimerization - Shell High Activity Catalyst. Se emplea para la producción de
homopolímeros y copolímeros al azar. Consiste en un reactor tanque agitado con
reciclo donde la polimerización se realiza en propileno líquido y se emplean
catalizadores con elevada actividad.
Proceso en masa con monómero en fase
gaseosa
Los procesos en fase gaseosa
aparecieron casi simultáneamente con los en fase líquida. Esta tecnología fue
revolucionaria porque evitaba completamente la necesidad de un solvente o un
medio líquido para dispersar los reactivos y productos del reactor. También
eliminaba la separación y recuperación de grandes cantidades de solventes o de
propileno líquido que era necesaria en los procesos con reactores en suspensión
o en fase líquida. El polipropileno producto que se obtenía en los reactores de
fase gas era esencialmente seco y sólo requería la desactivación de una pequeña
parte de los residuos del catalizador antes de la incorporación de aditivos y
su posterior peletización. Por lo tanto, esta tecnología redujo la manufactura
del polipropileno a pocos pasos esenciales. Algunos procesos representantes de
esta tecnología son: Novolen (BASF), Amoco – Chisso y
Unipol (Union Carbide).
El
proceso continuo Novolen (BASF) para producir homopolímeros,
copolímeros de impacto y al azar de propileno – etileno utiliza catalizadores
altamente
estereoespecíficos
y de elevada actividad. Los reactores están equipados con agitadores
helicoidales que proporcionan una excelente agitación. La homopolimerización
necesita únicamente un reactor primario donde se alimentan los componentes.
Éstos debe estar muy bien dispersos en el lecho particulado para evitar la
acumulación. Las condiciones de reacción son 70 – 80 ºC y 30 – 40 atm para
asegurar que el monómero se encuentre en fase gaseosa dentro del reactor. Para
controlar la masa molecular de polímero se emplean pequeñas concentraciones de
hidrógeno. La temperatura se controla extrayendo propileno gaseoso de la cámara
superior del reactor y condensándolo con agua de enfriamiento, y luego
recirculando hacia la parte inferior del reactor, donde su evaporación provee
el enfriamiento requerido, como así también la aireación del lecho agitado.
Cada tonelada de polímero producido requiere que se evaporen aproximadamente 6
toneladas de propileno líquido. La descarga continua de polvo y gas asociado
del reactor primario va directamente hacia un ciclón de baja presión. El gas
propileno portador de este ciclón se recircula hacia el reactor luego de
compresión, licuefacción, y algunas veces, destilación. El polvo pasa luego a
un recipiente de purga donde mediante un desactivador se apaga toda la
actividad del catalizador residual y el nitrógeno elimina trazas de propileno
del polvo caliente. Desde allí, el polvo se transporta hacia silos para su
estabilización y extrusión en gránulos.
Para
producir copolímeros de impacto, el polímero activo y el gas provenientes del
primer reactor se descargan directamente en el segundo (llamado
copolimerizador), que opera a 10 – 20 atm menos de presión y a menor
temperatura. Normalmente, la relación propileno/etileno/hidrógeno se ajusta de
tal manera que el copolímero gomoso del reactor tenga entre 40 – 60% en peso de
etileno. Esta composición gaseosa no puede condensarse sólo con agua, por lo
que se agrega una etapa de compresión para licuar parte del gas reciclado a la
base del reactor. El polvo del copolímero, con su gas portador, se descarga en
un separador ciclónico de baja presión, en el cual el gas portador pasa hacia
una recompresión y posteriormente regresas al copolimerizador. El monómero
residual del copolímero se remueve en un recipiente de purga y desactivación
antes de transportarlo a los silos para la extrusión.
El
proceso Amoco - Chisso utiliza un reactor agitado horizontal, en
vez del reactor agitado vertical del proceso BASF. El monómero reciclado
condensado se rocía por la parte superior del reactor y de esta manera provee
el enfriamiento necesario, mientras que el monómero no condensado y el
hidrógeno se inyectan por la base para mantener la composición del gas. Amoco
- Chisso afirman que su reactor alcanza algún grado de flujo pistón, más o
menos equivalente a 2 – 3 reactores de mezcla perfecta en serie. El proceso Unipol
(Union Carbide) combina las tecnologías de Union Carbide y Shell. Lo
más visible en este proceso, es el alto reactor de lecho fluidizado con su
sección superior expandida para reducir la velocidad del gas y el arrastre de
polvo. La alimentación continua de catalizador, hidrógeno y propileno se mezcla
continuamente en lecho fluidizado de fase densa del polvo. El calor de reacción
se remueve con un gran enfriador mediante un bucle de recirculación de gases.
En este sistema se dice que el lecho fluidizado se comporta como un reactor de
mezcla perfecta, sin la necesidad de separación de partículas gruesas. No se
requiere agitación mecánica. Las condiciones de reacción son < 88 ºC y <
40 atm, generalmente 70 ºC y 35 atm. El reactor de copolímeros de impacto
trabaja a la misma temperatura pero a presión más baja, aproximadamente 17 atm.
El
polvo de producto y el gas asociado se descargan justo debajo del plato
distribuidor por válvulas temporizadas hacia un separador ciclónico y luego
directamente a un recipiente de purga para remover el monómero residual. No se
necesita la remoción del catalizador ni la extracción del polímero atáctico
debido al uso de modernos catalizadores Shell en el proceso Unipol.
PROPILCO S.A (Proceso en fase gaseosa y lecho
fluidizado con tecnología UNIPOL)
Proceso Unipol
Etapa de almacenamiento y purificación
En la producción de homopolímeros se
emplea únicamente propileno, el cual es un hidrocarburo que llega a la planta
en estado líquido y a temperatura de - 44 ºC.
Este hidrocarburo arriba en buques y
se bombea desde el muelle hasta la planta para ser almacenado en dos esferas con
capacidad de 21000 toneladas, aisladas convenientemente para la conservación
del frío. En la producción de copolímeros random y copolímeros de impacto,
además de propileno se emplea el etileno. Este hidrocarburo, al igual que el
propileno, llega a la planta en buques, en estado líquido a - 106 ºC y se
almacena en un tanque cilíndrico debidamente aislado para su 14 conservación a
baja temperatura. El objetivo de mantenerlos a esta temperatura a fin de
controlar la alta volatilidad que presentan.
Posteriormente
de las esferas de almacenamiento se pasan los monómeros a cargar en el proceso
por un área de purificación, puesto que normalmente contienen impurezas tales
como agua, oxígeno, alcoholes, monóxido de carbono, etc., las cuales son
nocivas para el catalizador empleado en la reacción y por ende son retiradas
usando un tren de purificación especialmente diseñado para cada reactante. Los
equipos de remoción de impurezas, básicamente son tanques rellenos con tamiz
molecular. Cuando estos tamices se encuentran saturados de impurezas, se
regeneran con nitrógeno el cual se envía a la tea de la planta a fin de quemar
las trazas de impurezas. Los estándares de emisiones en la combustión de la tea
se consiguen controlando la intensidad de la llama por medio de inyección de
vapor, operación realizada desde la sala de control de la planta. La
polimerización del propileno es una reacción que requiere de una alta calidad
en las corrientes de alimentación, por lo cual es necesario remover todas las
trazas de contaminantes, dichos contaminantes pueden ser: H2O, H2S, CO2, COS,
NH3, PH3 y otros hidrocarburos oxigenados como alcoholes, cetonas y éteres,
etc. Una tecnología de separación efectiva y económica para la remoción de
estos contaminante es el uso de los adsorbentes selectivos. Se pueden utilizar
los tamices moleculares 4A, OG-941 y 13X de
la Union Carbide y F9 de la Mitsui, para la purificación de
propileno utilizado para la producción de polipropileno. Los tamaños promedio
de las aberturas de las cavidades de estos tamices son 0,4; 0,6; 1,0 y 0,9 nm,
respectivamente. En estos tamices se podrían retener impurezas de tamaño
molecular promedio menores de 1,0 o 0,9 nm, tales como H2O, CO2, CO, H2S y
mercaptanos.
El tamaño molecular promedio del
metanol es de 0,44 nm, mientras que el tamaño promedio de las aberturas de las
“cavidades” del tamiz molecular 4A es de 0,4 nm, por lo tanto
este adsorbente no puede retener el metanol presente en el propileno. En
pruebas de polimerización realizadas a escala piloto, se encontró que el
rendimiento obtenido del catalizador de TiCl4 con el propileno sin purificar es
de 14150 Kg de PP / Kg de catalizador. Cuando el propileno se purifica con las
tamices 4A, OG-941, 13X y F9 los
rendimientos obtenidos son de 18642, 19145, 22706 y 23034 Kg de PP / Kg de
catalizador, respectivamente. El tamiz molecular F9 como
adsorbente tiene un rendimiento ligeramente superior respecto al 13X.
Sin embargo, este último presenta una mayor porosidad, una menor densidad y un
mayor tamaño de abertura de cavidades, además su despacho es directamente desde
los Estados Unidos, mientras que el tamiz F9 proviene de Japón,
lo cual ocasionaría un retardo en su disposición inmediata.
Etapa de
reacción
Reactores
de polimerización
Con los monómeros purificados se pasa
a la zona de reacción, para la producción de homopolímeros y copolímeros
random. La reacción ocurre en fase gaseosa en un reactor de lecho fluidizado al
cual se alimentan continuamente los reactantes y un catalizador especialmente
diseñado para la obtención de polipropileno de configuración isotáctico. El
catalizador empleado pertenece al tipo Ziegler Nicholls,
específicamente tetracloruro de titanio y se mantiene almacenado en estado
líquido. Cuando pasa al proceso de reacción, experimenta un cambio de fase
convirtiéndose en gas para llevar a cabo la reacción en fase gaseosa con el
monómero (propileno). El sistema de reacción consta del reactor, un compresor
de desplazamiento positivo y un enfriador. El reactor tiene aproximadamente 40
metros de altura y 4 metros de diámetro. El compresor mantiene en circulación
continua los gases, succionando gases calientes del tope del reactor y
forzándolos a pasar a través de un enfriador para retornarlos por el fondo del
reactor. El polipropileno sólido formado se descarga continuamente hacia el
área de desgasificación. Las condiciones típicas de operación del reactor son
las siguientes: Carga: 20 ton/h a 40 ºC Temperatura de reacción: 65 ºC Presión
de reacción: 32 Kgf/cm2 Eficiencia o conversión: 96 – 97% Como se dijo
anteriormente dentro del reactor se tiene un lecho fluidizado. Este lecho está
formado por partículas del mismo producto, es decir polipropileno. La forma
geométrica del reactor, facilita el deslizamiento de las partículas fluidizadas
del lecho e impide que se vayan con las corrientes de reciclo gaseoso, el cual
es de aproximadamente 2000 lb/h. La capacidad del reactor en volumen para que
la reacción se desarrolle es de aproximadamente 500 metros cúbicos. El sistema
de la torre enfriadora utiliza aproximadamente un flujo de 12000 gal/min de
agua de enfriamiento tratada con molibdato. Para la producción de copolímeros
de impacto intervienen dos reactores instalados en serie. El sistema de
reacción Nº 2 al igual que el sistema de reacción Nº 1, está compuesto de un
reactor, un compresor y un enfriador. En el reactor Nº 1 se produce
homopolímero a partir de propileno y el catalizador; el polímero formado
(polipropileno homo) va al reactor Nº 2, donde la reacción prosigue, como una
mezcla de propileno y etileno.
Etapa
de desgasificación y peletizado
El
copolímero así formado se descarga al área de desgasificación. El polipropileno
descargado bien sea del reactor 1 o del 2, llega al tanque recibidor de
producto, acompañado de gases ricos en monómero. Los gases se ventean hacia el
sistema de recuperación, en el cual son comprimidos, enfriados y destilados. El
propileno monómero líquido se recicla a los reactores; si se está utilizando
etileno, éste se devuelve gaseoso al segundo reactor. La resina separada del
tanque recibidor de producto, pasa al tanque de purga. En este tanque se purgan
con una corriente de nitrógeno los pocos hidrocarburos que aún contiene el
polipropileno, la mezcla nitrógeno – hidrocarburos se ventea a la tea, donde
son quemados, la resina libre de hidrocarburos pasa al mezclador continuo donde
se funde y mezcla con aditivos para se sometida a peletización. La peletización
toma dos formas. Los cordones extruidos provenientes de la placa perforada de
la extrusora se enfrían con agua para dar filamentos rígidos. Luego cortadoras
de alta velocidad cortan los filamentos continuos entre 2 – 5 mm para producir
pellets. En el otro sistema, cuchillas de alta velocidad rotan contra la placa
perforada de la extrusora para cortar pequeñas longitudes del extruido fundido.
La temperatura de extrusión se encuentra entre 230 – 260 ºC. Los gases
venteados en el tanque recibidor de productos son ricos en monómeros y es
indispensable la recuperación del monómero (materia prima costosa), con el fin
de hacer más eficiente el proceso. Otra vez se recurre a la compresión,
enfriamiento y destilación, el polipropileno venteado se pasa de la fase
gaseosa a la líquida y se recircula a los reactores. Cuando se usa etileno,
éste se recircula hacia el sistema de reacción en estado gaseoso. Con el
propileno se encuentran trazas de propano. Este propano en pequeñas cantidades
es retirado en esta fase de purificación de la corriente de hidrocarburos y es
llevado como gas remanente a los equipos de combustión (calderas), con el fin
de ser quemado junto con el gas empleado por la planta.
Etapa
de almacenamiento y empaque
El
polipropileno peletizado y cortado, pasa por un elutriador, separando los finos
("off grade") y luego de la debida certificación de laboratorio es
llevado por transporte neumático a su almacenamiento en silos, despachándose a
clientes a granel por carros tolva, supersacos de 500 Kg, o en bolsas de 25 Kg.
Conclusiones
Los
procesos en fase gasosa evitan completamente la necesidad de un solvente o un
medio líquido para dispersar los reactivos y productos del reactor. También
eliminan la separación y recuperación de grandes cantidades de solventes o de
propileno líquido necesaria en los procesos con reactores en suspensión o en fase
líquida. La polimerización del propileno es una reacción que requiere de una
alta calidad en las corrientes de alimentación, por ende las impurezas, que son
nocivas para el catalizador empleado en la reacción, son retiradas usando un
tren de purificación especialmente diseñado para cada reactante. Los equipos de
remoción de impurezas, básicamente son tanques rellenos con tamiz molecular.
Para la purificación de propileno utilizado para la producción de polipropileno
se pueden utilizar los tamices moleculares 4A, OG-941 y
13X de la Union Carbide y F9 de la Mitsui. Sin
embargo, el tamiz molecular 13X como adsorbente presenta una
mayor porosidad, una menor densidad, un mayor tamaño de abertura de cavidades y
un alto rendimiento. Además se despacha directamente desde los Estados Unidos.
En el proceso Unipol (Union Carbide) implementado en PROPILCO
S.A., la reacción ocurre en fase gaseosa en un reactor de lecho fluidizado al
cual se alimentan continuamente los reactantes y un catalizador especialmente
diseñado para la obtención de polipropileno de configuración isotáctico. Ese
catalizador empleado pertenece al tipo Ziegler Nicholls,
específicamente tetracloruro de titanio y se mantiene almacenado en estado
líquido. Cuando pasa al proceso de reacción, experimenta un cambio de fase
convirtiéndose en gas para llevar a cabo la reacción en fase gaseosa con el
monómero (propileno).
Proceso de deshidrogenación
Las olefinas son por lejos más reactivas
que las parafinas por los enlaces tipo π, termodinámicamente el hidrógeno
reacciona con la olefinas para formar parafinas. Esta reacción es más fácil que
se de a cabo que la reacción inversa por la reactividad de las olefinas, por
ello las reacciones de deshidrogenación requieren de temperaturas mayores que
las reacciones de hidrogenación y por ende mayor cantidad de energía.
Los
hidrocarburos de bajo peso molecular frecuentemente son convertidos a olefinas
a través de los procesos de craqueo térmico. Para el proceso de
deshidrogenación es necesaria la presencia de catalizadores ya sea de platino o
paladio en la deshidrogenación de hidrocarburos de cadena lineal C5-C8, la
clave para el uso del catalizador es de disminuir o prevenir reacciones no
deseadas como de isomerización y aromatización.
Teoría de la deshidrogenación
La deshidrogenación es una clase reacción
química en el cual se obtienen compuestos menos saturados y más reactivos.
Existes muchos procesos de conversión en donde el hidrógeno es removido,
principalmente porque todo compuesto que contenga hidrógeno puede ser
deshidrogenado, aunque los hidrocarburos y alcoholes son los compuestos más
comunes, con el fin de obtener olefinas, cetonas, y otros compuestos orgánicos.
Esta reacción se aplica a nivel industrial en refinerías e industrias
petroquímicas.
Las reacciones de deshidrogenación son muy
difíciles de darse ya que requieren de altas temperaturas para favorecer el
equilibrio así como velocidades de reacción adecuadas. Son reacciones
endotérmicas que requieren entre 15-35 kcal/gmol de energía. El uso de
catalizadores activos es necesario, además del proceso de regeneración para
remover el coque depositado en la superficie del catalizador.
El calor requerido puede ser introducido a través de
banco de tubos de (5 a 15 cm) para precalentar la corriente de alimentación a
los reactores. Cuando el gradiente de temperatura es elevado, la transferencia
de calor ocurre desde el exterior de los tubos hacia el interior de los mismos.
Uno de los problemas que tiene ese proceso
es que los cambios de temperatura ocurren en un tiempo muy corto para prevenir
reacciones secundarias, además de que las caídas de presión son bajas
en el lecho catalítico y la selección del material del reactor puede resistir
las condiciones de operación.
Simulación de deshidrogenación de propano a propileno en un reactor de flujo radial-sobre Pt-Sn / Al2O3 como catalizador
Deshidrogenación de parafina catalítico para olefinas de fabricación se considera que es una de las rutas de producción más importante en las industrias petroquímicas. Un modelo cinético reactor para la deshidrogenación de propano a propileno en un reactor de flujo radial sobre Pt-Sn / Al2O3 como catalizador fue investigado aquí. El modelo mostró que la actividad del catalizador era altamente dependiente del tiempo. Además, las concentraciones de los componentes y la temperatura varía a lo largo del radio del reactor debido a la reacción endotérmica se produzcan. Por otra parte, una tendencia similar se observó para la conversión de propano como la selectividad de propileno, con ambos decreciente durante el periodo de tiempo estudiado. Además, una inversión de esta tendencia también se pone de manifiesto cuando se mejoró la temperatura de alimentación o cuando se añadió argón en la alimentación como un gas inerte.
PROPILENO REACTOR..
PROPILENO REACTOR..
Bibliography
1. Chemical Engineering Department-Auburn University-CHEN 4460- Mario
Richard Eden INTRODUCTION
TO ASPEN PLUS SIMULATION
2.
Gerardo Muñoz -Business Consultant -Aspen Technology,
Inc. Optimice
todo el proceso químico con Aspen Plus
3.
Sharif University of Technology-Scientia
Iranica-Transactions C: Chemistry and Chemical
Engineering-www.sciencedirect.com-Kinetic
modeling of side reactions in propane dehydrogenation over Pt-Sn/γ Al2O3
catalyst
4. Sharif
University of Technology-Scientia Iranica-Transactions
C Chemistry and Chemical Engineering-www.sciencedirect.com-Kinetic
modeling of side reactions in propane dehydrogenation over Pt-Sn/γ Al2O3 catalyst
5. Simulation of Propylene
Polymerization in Industrial-Reactors Using Ziegler-Natta Catalysts in the
-Presence of Electron Donors-Ahmad Alshaiban, Joao B. P. Soares
6. Reacción-Deshidrogenación de Propano
Kinetic modeling of propane dehydrogenation over an industrial catalyst in the
presence of oxygenated compounds-Bijan Barghi • Moslem Fattahi • Farhad
Khorasheh
7. PROPYLENE
8. ZIEGLER-NATTA CATALYSTS Available on line at Association of the
Chemical Engineers of Serbia AChE www.ache.org.rs/CICEQ Chemical Industry & Chemical Engineering
Quarterly 19 (1) 13−24 (2013) COMPARATIVE SIMULATION STUDY OF GAS-PHASE
PROPYLENE POLYMERIZATION IN FLUIDIZED BED REACTORS USING ASPEN POLYMERS AND TWO
PHASE MODELS
9. Modeling of Solid–Liquid Equilibria
for Polyethylene and Polypropylene Solutions with Equations of State G. M. N.
Costa,1 S. Kislansky,1 L. C. Oliveira,1 F. L. P. Pessoa,2 S. A. B. Vieira de
Melo,1M. Embiruc¸u1 Received 9 May 2010; accepted 4 August 2010 Published
online 10 March 2011 in Wiley Online Library (wileyonlinelibrary.com).
10. Revista Facultad de Ingeniería N. 33. pp. 52-57. Junio, 2005
Deshidrogenación oxidativa de propano utilizando molibdato de mangane Juan
Carlos Echavarría Vera*, Luz Amparo Palacio Santos* (Recibido el 26 de abril de
2004. Aceptado el 11 de marzo de 2005)
11. Catalytic Dehydrogenation of Propane
by Carbon Dioxide: A Medium-Temperature Thermochemical Process for Carbon
Dioxide Utilisation X. Du,a B. Yao,b S. Gonzalez-Cortes,a V. L. Kuznetsov,a
Hamid AlMegren,c T. Xiao,a* P. P. Edwards,
12. Polymer-Plastics Technology and
Engineering Publication details, including instructions for authors and
subscription information: http://www.tandfonline.com/loi/lpte20
Preliminary Design of a Loop Reactor for Bulk Propylene Polymerization Monica
A. Ferrero a & Mario G. Chiovetta a a INTEC CONICET – Universidad Nacional
del Litoral Guemes 3450, (3000) Santa Fe, Argentina Published online: 23 Oct
2006.
13. The Catalytic Polymerization of
Propylene FREDERICHK. GAYER,G eneral Motors Research Laboratories, Detroit,
Mich.
14. Molecular Simulation of
Propane-Propylene Binary Adsorption Equilibrium in Zeolite 13X Miguel A.
Granato,† Thijs J. H. Vlugt,‡ and Alı´rio E. Rodrigues, Laboratory of
Separation and Reaction Engineering (LSRE), Department of Chemical Engineering,
Faculty of Engineering, UniVersity of Porto, Rua Dr. Roberto Frias, s/n,
4200-465, Porto, Portugal, and Condensed Matter and Interfaces, Utrecht
UniVersity, P.O. Box 80.000, 3508 TA Utrecht, The Netherlands.
15. Sim Yee Chin, Anwaruddin Hisyam and
Haniif Prasetiawan Modeling and Simulation Study of an Industrial Radial Moving
Bed Reactor for Propane Dehydrogenation Process.
16. PROPYLENE = POLYMERIZATION e Under
High Pressure and Temperature with and without Phosphoric Acid
17. MgCl2-Supported Ziegler–Natta
Catalyst Containing Dibenzoyl Sulfide Donor for Propylene Polymerization Ga-Hee
Kim,1 Byung-Hwan Um,1 Ki-Chul Son, Kyeongseok Oh Hyoung Lim Koh
18. Accepted Manuscript Title: Dynamic
simulation of liquid polymerization reactors inSheripol process for
polypropylene Author: Shin Hyuk Kim Seung Won Baek Jae Cheol Lee Seong Uk Hong
Min Oh PII: S1226-086X(15)00462-1
Reference: JIEC 2686 To appear in: Received
date: 19-8-2015 Revised date: 13-10-2015 Accepted date: 14-10-2015
19. Kinetic model and Simulation
Analysis for Propane Dehydrogenation in an Industrial Moving Bed Reactor Chin
S. Y., Radzi, S. N. R., Maharon, I. H. and Shafawi, M. A.
20. Ziegler-Natta catalysts for
propylene polymerization: Chemistry of reactions leading to the formation of
active centers
21. Effect of potassium addition on
bimetallic PtSn/h-Al2O3 catalyst for dehydrogenation of propane to propylene Mi-Hyun
Lee1,3 Bhari Mallanna Nagaraja4 Prakash Natarajan5 Ngoc Thanh Truong1,2Kwan
Young Lee Sungho Yoon5 Kwang-Deog Jung1,2
22. Kinetics of propane dehydrogenation
over Pt–Sn/Al2O3 catalyst Qing Li a, Zhijun Suia, Xinggui Zhoua,∗, De Chenb,a State Key Laboratory of Chemical Engineering, East China
University of Science and Technology, Shanghai 200237, China b Department of
Chemical Engineering, Norwegian University of Science and Technology (NTNU),
Sem SŁlandsvei 4, N-7491 Trondheim, Norway
23. Modeling and Simulation of Liquid
Phase Propylene Polymerizations in Industrial Loop Reactors Eneida A. de
Lucca,1 Rubens Maciel Filho,1 Prı´amo A. Melo,2 Jose´ Carlos Pinto
24. Monte Carlo Simulation of Propylene
Polymerization ( I ) Effects of Impurity on Propylene Polymerization LUO
Zhenghong(Y iE CAO Zhikai and SU Yaotang
Department of Chemical and Biochemical
Engineering, Xiamen University, Xiamen 361005, China
25. Ethylene and propylene
polymerization catalyzed by a model Ziegler-Natta catalyst prepared by gas
phase deposition of magnesium chloride and titanium chloride thin films E.
Magni b and G.A. Somorjai a,ba Department of Chemistry and b Materials Sciences
Division,Lawrence Berkeley National Laboratory, University of California,
Berkeley, CA 94720, USA Received 16 July 1995; accepted 23 August 1995
26. Kinetics of Ethylene-Propylene
Copolymerization G. NATTA, G. MAZZANTI, A. VALVASSORI, G. SARTORI, and A. BARBAGALLO,
Istituto di Chimica Industriale del Politecnico, Milan, Italy
27. Study of Propane Dehydrogenation to
Propylene in an Integrated Fluidized Bed
Reactor Using Pt-Sn/Al-SAPO-34 Novel
Catalyst Zeeshan Nawaz, Yue Chu, Wei Yang, Xiaoping Tang, Yao Wang, and Fei Wei
Beijing Key Laboratory of Green Chemical Reaction Engineering & Technology
(FLOTU), Department of
Chemical Engineering, Tsinghua
UniVersity, Beijing 100084, China
28. Modeling of Coke Formation and Catalyst
Deactivation in Propane Dehydrogenation Over a Commercial Pt-Sn/γ-Al2O3
Catalyst S. Niknaddaf a , M. Soltani b , A. Farjoo a & F. Khorasheh a
Department of Chemical and Petroleum Engineering , Sharif University of
Technology , Tehran , Iran b National Iranian Petrochemical Company, Research
and Technology Division , Tehran , Iran Published online: 30 Oct 2013.
29. Polymerization of liquid propylene
with a 4th generation Ziegler–Natta catalyst—in+uence of temperature, hydrogen
and monomer concentration and prepolymerization method on polymerization
kinetics Jochem T. M. Patera; G2unter Weickertb, Wim P. M. van Swaaijb aBP
Chemicals SNC, Research and Technology Center, Ecopolis Lavera Sud, P.O. Box 6,
F-13117 Lavera, France
B High Pressure Laboratories,
Process Technology Institute Twente, University of Twente, P.O. Box 217, NL-7500AE
Enschede, The Netherlands Received 9 November 2001; accepted 15 January 2002
30. Polipropileno Industrias Petroquímicas Trabajo de investigación sobre el polipropileno como producto
petroquímico. Cristian Fabián González 28/09/2010
31. Polypropylene Production
Optimization in Fluidized Bed Catalytic Reactor (FBCR): Statistical Modeling
and Pilot Scale Experimental Validation Mohammad Jakir Hossain Khan 1, Mohd
Azlan Hussain 1,2,* and Iqbal Mohammed Mujtaba 3 1 Department of Chemical
Engineering, Faculty of Engineering, University of Malaya, 50603 Kuala Lumpur,
Malaysia; E-Mail: jakirkhanbd@gmail.com
2 UM Power Energy Dedicated Advanced Centre (UMPEDAC); Wisma R & D,
University of Malaya, 59990 Kuala Lumpur, Malaysia 3 Chemical Engineering
Division, School of Engineering, University of Bradford, Bradford BD7 1DP, UK;
E-Mail: I.M.Mujtaba@bradford.ac.uk
Author to whom correspondence should be addressed.
32. Procesos de fabricación de polipropileno Obtención del Polipropileno
33. PRODUCCIÓN DE POLIPROPILENO PROCESOS PETROQUÍMICOS INGENIERO QUÍMICO
ORLANDO CASTIBLANCO URREGO
34. Modeling and Simulation of Propylene
Polymerization in Nonideal Loop Reactors A. S. Reginato, J. J. Zacca, and A. R.
Secchi Dept. of Chemical Engineering, UFRGS, Porto Alegre, RS, Brazil, CEP
90050-170
35. Simulation of propylene
polymerization: an efficient algorithm Priyabrata Sarkar and Santosh K. Gupta Department
of Chemical Engineering, Indian Institute of Technology, Kanpur-208016, India (Received
24 September 1990; revised 6 February 1991; accepted 19 March 1991)
36. Propylene Hydrogenation and Propane
Dehydrogenation by a Single-Site Zn2+ on Silica Catalyst Neil M. Schweitzer,,
Bo Hu, Ujjal Das, Hacksung Kim, Jeffrey Greeley Larry A. Curtiss, Peter C.
Stair, Jeffrey T. Miller and Adam S. Hock
37. A Kinetic Model for Ethylene
Polymerization with a Polymer Supported Ziegler-Natta Catalyst A. Shariati,
C.C. Hsu & D.W. Bacon To cite this article: A. Shariati, C.C. Hsu &
D.W. Bacon (1999) A Kinetic Model for Ethylene Polymerization with a Polymer
Supported Ziegler-Natta Catalyst, Polymer Reaction Engineering, 7:1, 97-130
38. Mechanism of Propylene
Polymerization with MgCl2‑Supported Ziegler−Natta Catalysts Based on Counting of Active Centers:
The Role of External Electron Donor Xian-rong Shen, Zhi-sheng Fu, Jie Hu, Qi
Wang, and Zhi-qiang Fan*
MOE Key Laboratory of Macromolecular
Synthesis and Functionalization, Department of Polymer Science and Engineering,
Zhejiang University, Hangzhou 310027, China
39. Propylene Propane Separation by
Vacuum SwingAdsorption Using 13X Zeolite
Francisco A. Da Silva and Alirio E.
Rodrigues Laboratory of Separation and Reaction Engineering, Dept. of Chemical
Engineering, University of Porto, 4200-465 Porto, Portugal
40. Polypropylene production simulation
with cape-open interfacing of pro/ii and gPROMS Article in Journal of
Engineering Science and Technology · January 2015
41. An insight into the
chain-propagation mechanism of propylene polymerization catalyzed by
traditional Ti-based Ziegler–Natta catalysts in view of recently developed
catalysts TIANXU SUN, LI WANG∗, XIAOCHEN DONG and WEI WANG State
Key Lab of Polymer Reaction Engineering, Zhejiang University, Hangzhou 310027,
People’s Republic of China
42. POISONING OF ACTIVE SITES ON
ZIEGLER-NATTA CATALYST FOR PROPYLENE POLYMERIZATION Kitti Tangjituabun, Sang
Yull Kim, Yuichi Hiraoka, Toshiaki Taniike and Minoru Terano* School of
Materials Science, Japan Advanced Institute of Science and Technology, Ishikawa
923-1292, Japan Bunjerd Jongsomjit and Piyasan Praserthdam Department of
Chemical Engineering, Chulalongkorn University, Bangkok 10330, Thailand
43. Propylene Hydrogenation over
Platinum/Carbon Molecular Sieve Catalysts D. L. TRIMM Departme& of Chemical
EtLginee,ing rind Chemical l’echnology, Imperial College, London, S.11. 7,
Errgland
44. Dehydrogenation of Propane Using a Packed-Bed
Catalytic Membrane Reactor Herman Weyten, Klaas Keizer, Annemieke Kinoo, Jan
Luyten, and Roger Leysen Flemish institute for Technological Research, Process
Technology, Boeretang 200, B-2400 Mol, Belgium
45. Oxidative dehydrogenation of propane
for propylene production comparison of
catalytic processes D. Wolf , N. Dropka, Q. Smejkal, O. Buyevskaya Institute
for Applied Chemistry, Berlin-Adlershof, Richard-Willsta( tter-Str. 12, D-12489
Berlin, Germany
46. Gas Phase Ethylene Polymerization:
Production Processes, Polymer Properties, and Reactor Modeling Tuyu Xie, Kim B.
McAuley,' James C. C. HSU, and David W. Bacon Department of Chemical
Engineering, Queen's University, Kingston, Ontario, Canada K7L 3N6
47. Petroleum Science and Technology Publication
details, including instructions for authors and subscription information: http://www.tandfonline.com/loi/lpet20
Kinetics of Propane Oxidative
Dehydrogenation to Propylene Hongjun You a State Key Laboratory of Heavy Oil ,
University of Petroleum , Changping, Beijing, P.R. China Published online: 14
Feb 2007.
48. Propane dehydrogenation to propylene
over Pt-based catalysts Changlin Yu, Qingjie Ge, Hengyong Xu,* and Wenzhao Li Natural
Gas Utilization, Applied Catalysis Laboratory, Dalian Institute of Chemical
Physics, Graduate School of the Chinese Academy of Sciences, 457 Zhongshan
Road, Dalian, 116023, P.R. China
49. Size-Dependent Reaction Mechanism
and Kinetics for Propane Dehydrogenation over Pt Catalysts Jun Zhu, Ming-Lei
Yang, Yingda Yu, Yi-An Zhu, Zhi-Jun Sui, Xing Gui Zhou, Anders Holmen, and De
Chen
Aspen Polymers v 8.4
- M. Saravanan Khalid 2014. A Study on the Process Plant Design for Production of Polypropylene Plant, Department of Mechanical and Industrial Engineering, Caledonian college of Engineering: https://drive.google.com/file/d/0B8m-EIyYJnhjS1MwNHhhQmZkbTQ/view?usp=sharing
- Harutun G. Karian 1999 Hambook of Polypropylene and Polypropylene composites: https://drive.google.com/file/d/0B8m-EIyYJnhjUm52VHB1WnhSSG8/view?usp=sharing
- Edward P., Jr. Moore Polypropylene Handbook: Polymerization, Characterization, Properties, Processing, Applications [1 ed.] Hanser Gardner Publications: https://drive.google.com/file/d/0B8m-EIyYJnhjZV9uekNEV0xoUTg/view?usp=sharing
- Devesh Tripathi, 2002 Practical Guide to Polypropylene: https://drive.google.com/file/d/0B8m-EIyYJnhjb3lyUjVDSGQxd28/view?usp=sharing
- Ullmann's Encyclopedia of Industrial Chemistry T. GEOFFREY HEGGS, current address: The Mill, Great Ayrton, TS9 6PX, Polypropylene United Kingdom: https://drive.google.com/file/d/0B8m-EIyYJnhjZV9uekNEV0xoUTg/view?usp=sharing
- Produccion de Polimeros: https://drive.google.com/file/d/0B8m-EIyYJnhjZHp0UWJsbmtGUGc/view?usp=sharing
- Kirk-Othmer Encyclopedia of Polypropylene: https://drive.google.com/file/d/0B8m-EIyYJnhjMlY2R09PX2x5OEE/view?usp=sharing





































4 comentarios:
Información Artículos científicos sobre el proceso de planta de propileno y Polipropileno
http://www.mediafire.com/download/9xwtv3z8l9hf7c6/Paper+Propileno.zipx
http://www.mediafire.com/download/7m4cx9oq2jkuhky/Aspen+Plus.zipx
Que buena información, muy cmpleto el post.
Yo acabo de adquirir una Bomba Polipropileno y me va bastante bien con ella.
saludos!
Yo ando buscando una Valvula de Polipropileno... supongo que tambien la tienen
Publicar un comentario